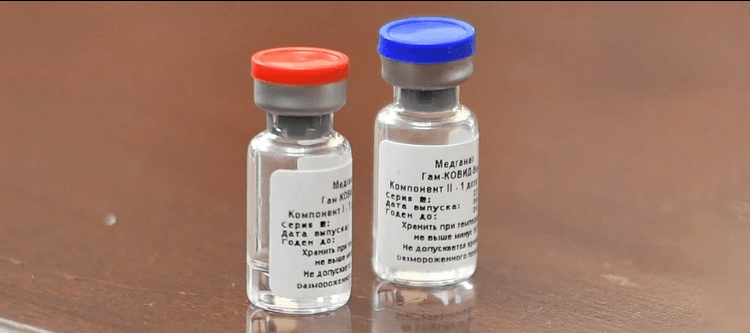
8月11日,俄罗斯政府宣布批准世界上首个新冠肺炎疫苗注册。由于该疫苗尚未通过临床第三阶段试验,因此在世界各地的科学家中引起了广泛的争议。世界卫生组织表示,它期待着对俄罗斯的临床试验进行审查。
据报道,俄罗斯的疫苗只被世界卫生组织列为疫苗的第一阶段。"世界卫生组织(WHO)正在与俄罗斯科学家和当局联系,并期待着审查实验的细节,"该机构在一份声明中说。自今年一月以来,世界卫生组织(世卫组织)一直参与指导和加速疫苗的研究和开发。加速疫苗研究应遵循既定程序,并在每一步进行,以确保每一种疫苗最终进入生产和销售是安全和有效的。一种安全有效的流行病疫苗将是一种全球公益物,世界卫生组织(世卫组织)敦促在全球范围内迅速、公平和公平地获得这种疫苗。"&
在由ClinicalTrials.gov发布的两项临床1/2研究中,有少量数据显示,总共有38名患者接受了实验疫苗治疗。这是76项研究中的38项,还是两项研究中的38项。研究对象的数量远远低于其他第三阶段临床研究,包括阿斯利康(AstraZeneca)、现代疫苗(Modizer)、辉瑞(Pfizer)和其他新冠肺炎候选疫苗研究。
TrialScope首席战略官托马斯·威克斯(ThomasWicks)表示,俄罗斯境外已知数据的透明度似乎不完整,尤其是一种已获批准供公众使用的药物,而且很难从38名参与者那里得出安全和有效的结论。俄罗斯政府宣布批准后,将在稍后阶段继续进行临床第三阶段试验,作为确认试验。韦克斯认为,与传统的对照研究不同,以后的研究可能会继续追踪接种人群以确定安全性和有效性。这一批准相当于一场有偿赌博,我们都希望它是安全和有效的。
GlobalData高级传染病分析师菲利普·罗森鲍姆(Philippenbaum)认为,疫苗可能还有其他因素。美国和中国的监管机构一致认为,安全有效性研究需要比在俄罗斯进行的时间更长。疫苗制造商需要披露自己的数据,以便所有人都能看到。有很多反疫苗阴谋论,如果疫苗失败,它将加剧火灾。
在美国,如果临床第三阶段的临时数据支持有效性和安全性,FDA就可以授予紧急使用授权,"威克斯说。也许俄罗斯加快了紧急授权的审批过程,就像FDA对Redsievere和羟氯喹的审批一样,所以不要太担心。如果没有证据表明疫苗有效,比如羟基氯喹,取消紧急批准。